包括病理学分野での大きな目標は、白血病・リンパ腫・腫瘍など多くの難治性疾患の理解と克服です。研究では、患者さんが研究の起点となり、研究のゴールも患者さんを助けることです。
疾患とその重症度を見極める病理診断の基盤を活かし、病理=切片というクラシカルな取り組みを大事にしながら、sequencing, computation, drug discoveryに至るまで、専門分野を超えて患者さんを助け支えるmotivationを共有し、皆で多様なscience and technologyを取り入れ、研究しています。「疾患克服に挑戦する気持ち=助ける病理学」を、スタッフから学生まで、世代を超えて共有します。
同じ診断でも、病勢や治療への応答性が異なるのが、ベッドサイドのreal worldであり、1. Humanized Mouseやpatient-derived xenograftと呼称されるシステムで、生体内での正常・疾患いずれもヒト細胞のdynamicsを知る、2. 個体から、各組織/臓器、細胞、蛋白、遺伝子、代謝物など、複数の階層を繋ぐように網羅的な計測を行い、dataからdiseaseの本質や弱点を見つけ出す、を重要視しています。スタッフは、皆、それぞれに理解したいと願う疾患、助けたいと思う患者さんを思い浮かべ、専門の分野を持っていきます。病理という世界だけで研究するのではなく、多くのコラボレーターと仕事をしており、その方々の元で学ぶことも奨励します。学部生でも大学院生でも医師でも、世界を知る・視る、素晴らしき人に出会う、その繋ぎの役割も担います。また、ビジネスディベロプメントの世界とcollaborateすることで、新しい治療を開発して患者さんの元へと届ける仕組みについて、国内外で取り組んでいます。共同研究者についても紹介しますので、医科歯科と各所を行き来しながらリサーチすることも、視野を広げ、研究を深め、夢を叶える良い方法かもしれません。
1. ヒト血液・免疫・疾患の再現
上記の通り、患者さんそれぞれに疾患の様子も違えば、それを抑えようとする免疫の力も異なります。免疫は、造血幹細胞から作られ、その過程をマウスに再現しながら、どのような遺伝子があれば、強い免疫を作ることができるか、また、白血病が骨で発生して、どのように全身に拡がり、それを阻止できる治療は何かを研究しています。助ける研究には、多様な考えや研究ツールが必要です。
-
1a. Nature Biotechnology 2007「患者白血病状態を再現。抗がん剤治療に抵抗性を示す白血病細胞の局在を同定」
-
1b. Nature Biotechnology 2010「一部の白血病細胞の細胞周期がG0(静止期)にあることが治療抵抗性・再発の原因に」
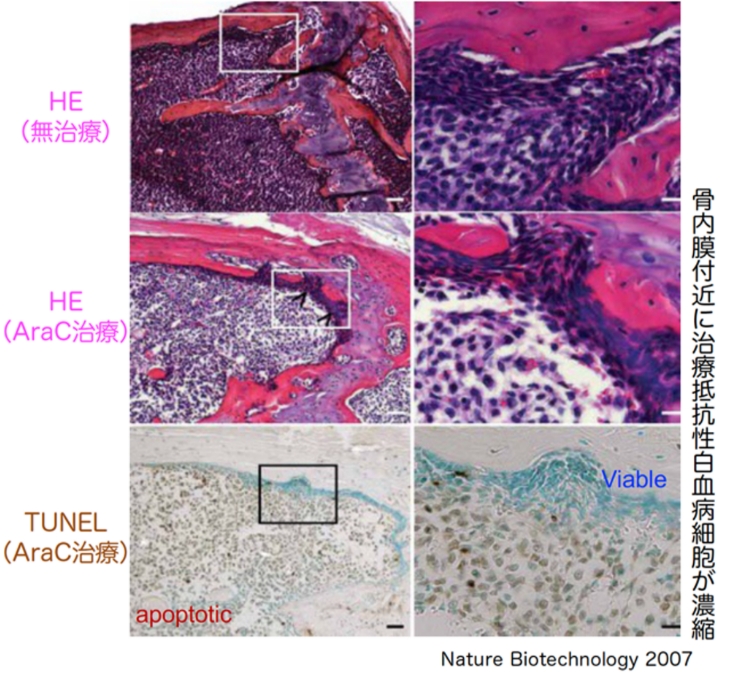
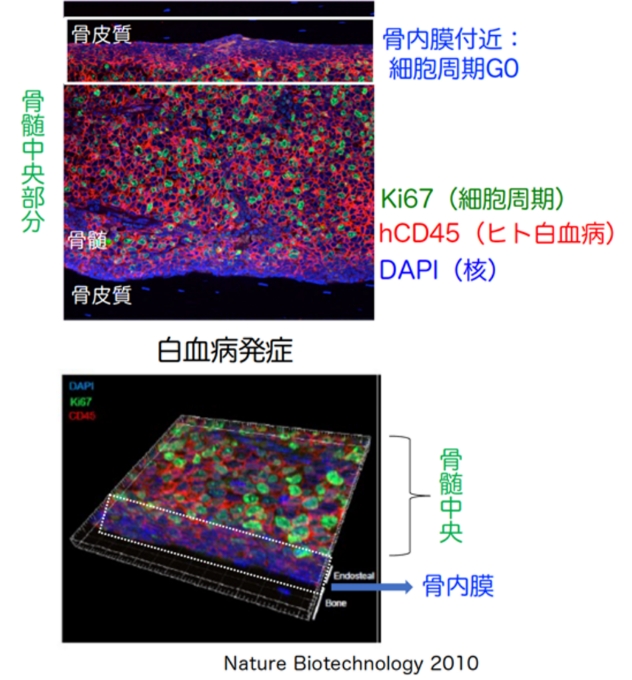
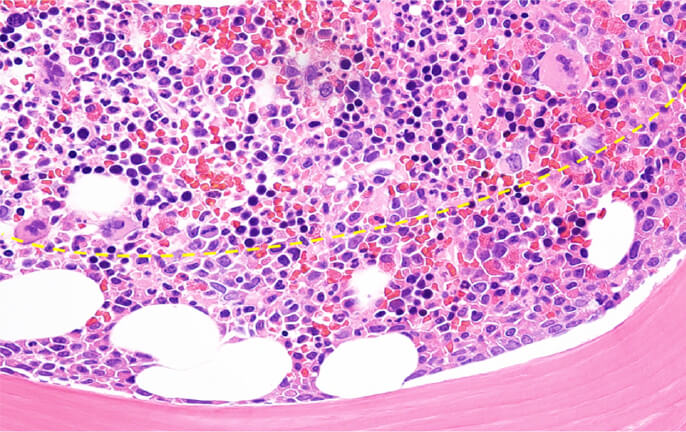
白血病患者さんの細胞にて、病気を再現。骨髄と骨皮質の境界付近に治療抵抗性の白血病細胞が存在し、
これらは細胞周期が静止期 (GO)にある。これらの中に治療標的分子を見出す研究を進めている。
2. 白血病再発の理解と治療開発
一旦、化学療法などで減少した白血病細胞が再び増えてくる「再発」を根絶するのが、私たちの大きな目標です。そのために、再発の原因となる細胞を見出し、その中に治療標的を同定して治療を作る。このような取り組みを、多数の患者さんの思いと共に進めてきました。白血病を追い詰めるように連続性を持って研究を進める姿勢と、進めながら、私たちも、変化するテクノロジーを学びつつ、より素晴らしいチームワークを構築する思いを持っています。
-
2a. Science Translational Medicine 2010「患者白血病の治療標的の同定」
-
2b. Science Translational Medicine 2013「白血病のリン酸化酵素阻害による治療の提案」
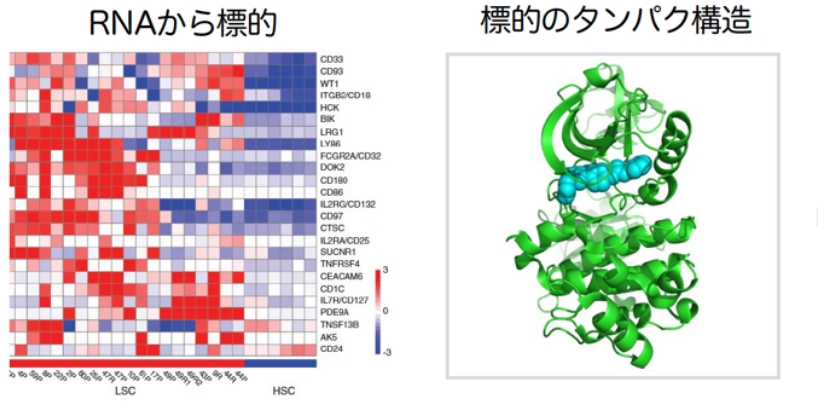
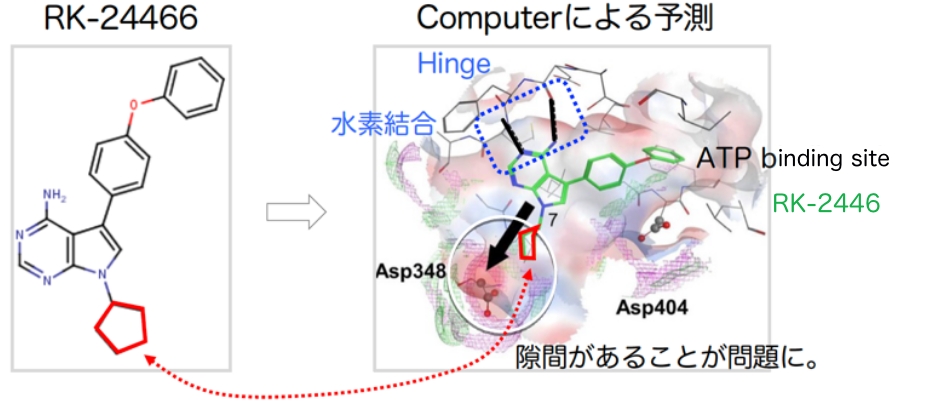 より良い化合物の合成
より良い化合物の合成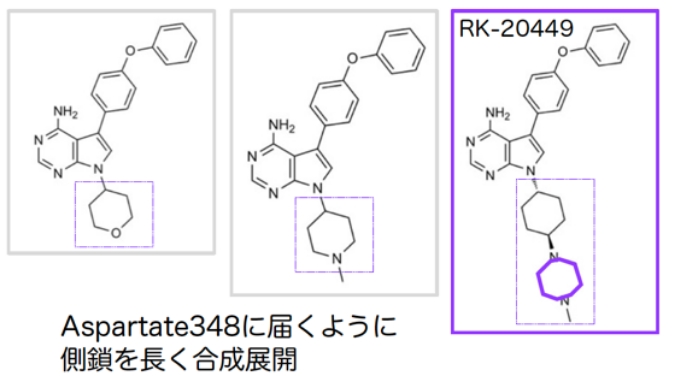 X線立体構造解析(実測)
X線立体構造解析(実測)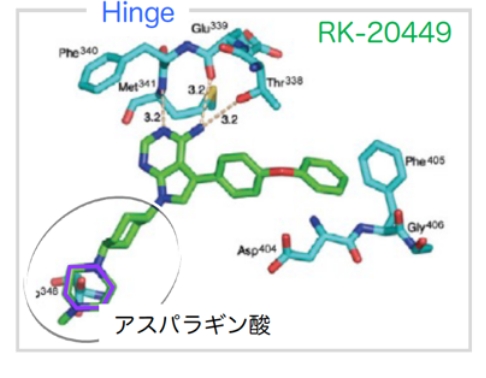 患者白血病細胞への効果検証
患者白血病細胞への効果検証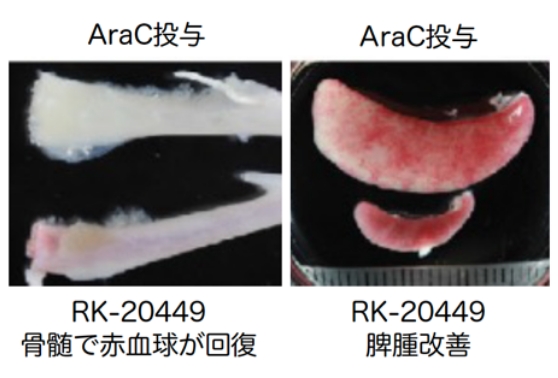
-
2c. Science Translational Medicine 2017「1細胞解像度でのDNA sequencingと腫瘍特異的変異の同定」
-
2d. Nature Cancer 2021「白血病根治を目指す個別最適化治療」
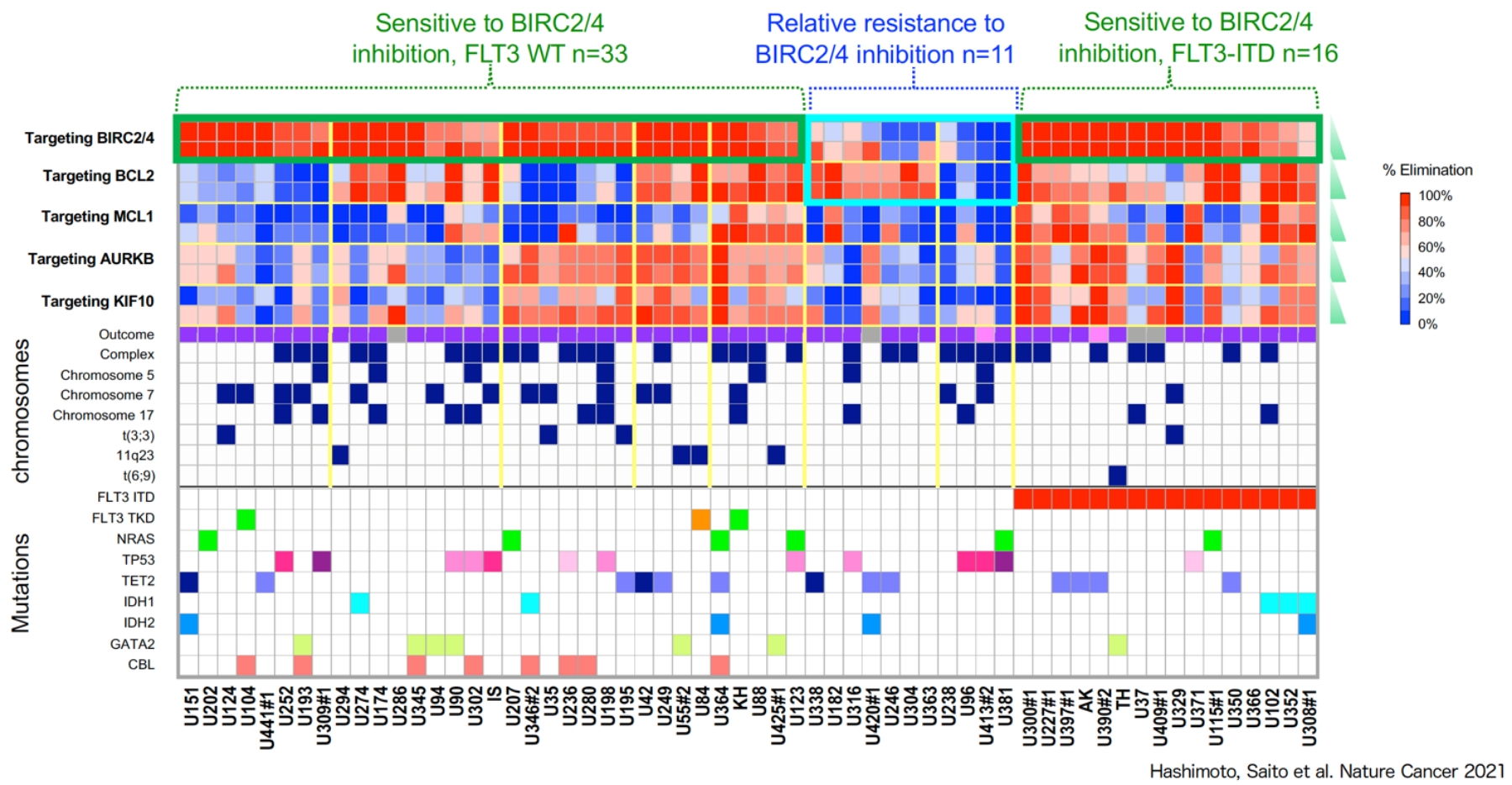
3. 骨髄微小環境の可視化
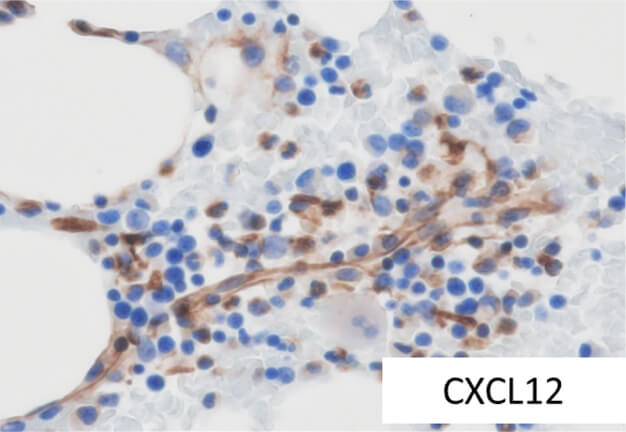
ヒト骨髄における骨髄微小環境の
病理学的評価
血液学で知られている骨髄微小環境を光学的顕微鏡でとらえるには何か必要か?分子生物学的な側面からもアプローチする。
ランダム変異を用いた骨髄微小環境の構築
~がん微小環境における細胞間相互作用の理解~
これまでの「がん微小環境」に関する多くの報告が主に予後不良のがんそのものを主体とした研究であったことに対し、本研究チームでは、包括的に腫瘍周囲支持細胞による薬剤耐性誘導のメカニズムを解明するために、新たなCRISPR screening法※3の確立を行いました。
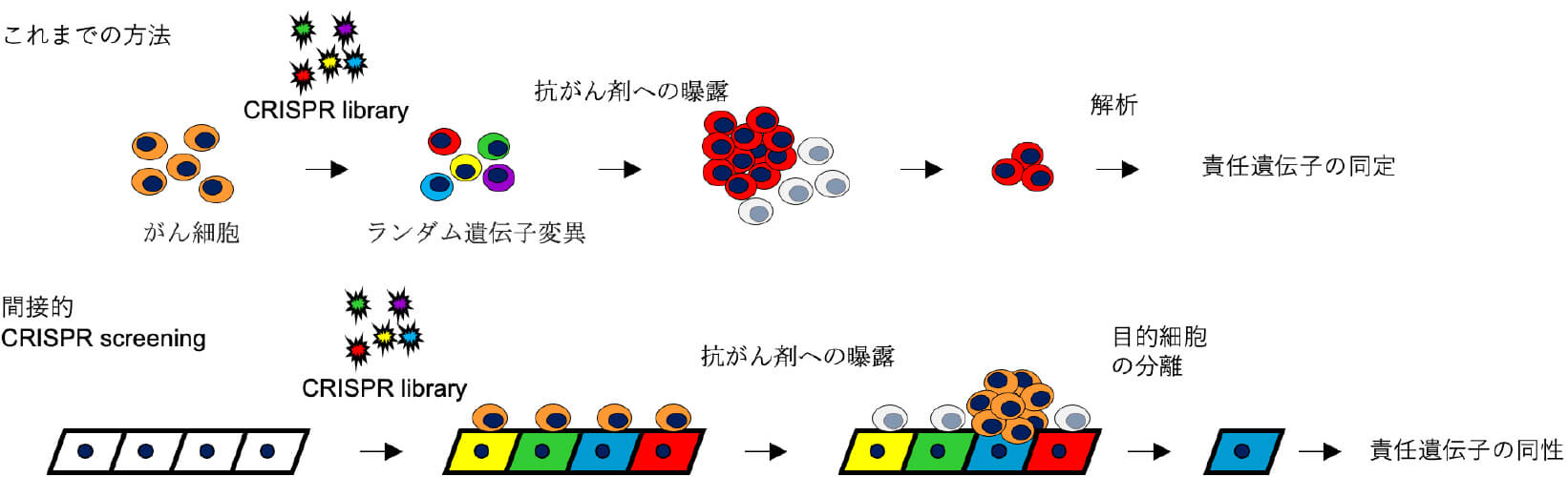
Sugita K et al. 2023
Communications biology
4. 乳がん、膵内分泌腫瘍、子宮内膜症、脂肪肉腫、悪性中皮腫など、幅広い疾患を対象とする病理学・医学の深化。疾患細胞・間質の関係性の可視化。
血液系の腫瘍だけを研究している訳ではありません。病理スタッフが取り組んできた仕事は、さらなる進化を遂げています。
以下、みていただけたら幸いです。
研究業績
業績の詳細については以下のページからご覧ください。
- 国立大学法人 東京科学大学


